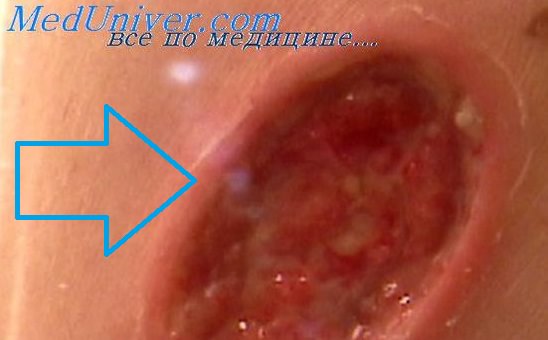
Десмопластическая реакция что это
Десмопластическая меланома является одним из вариантов узловой меланомы или меланомы стадии вертикального роста. Состоит из веретенообразных клеток и отличается выраженной десмопластической реакцией стромы. Если присутствует стадия радиального роста, то это обычно один из лентигинозных типов меланомы. Это необычный вариант меланомы, который выглядит как непигментированное образование на коже, подобное шраму или рубцу, но без предшествующего травматического повреждения в анамнезе Если биопсия взята поверхностно, образование можно принять за келоид или дерматофиброму. Так как нет четких клинических проявлений, характерных для мела-номы, очень большое значение имеет анамнез. В вертикальной стадии роста десмопластическая меланома принимает вид твердого узла, также беспигментного или слабопигментированного.
Микроскопически десмопластическая меланома состоит из веретенообразных клеток, расположенных между тонкими прослойками коллагена. Ядра клеток вытянутые, S-образные, подобно клеткам в нейрофибромах или шванномах. Часто клетки сгруппированы в пучки. В более поверхностных отделах могут встречаться эпи-телиоидные клетки, единичные или сгруппированные в гнезда. Если в опухоли есть пигмент, то скорее он будет в эпителиоидных клетках. Описаны поля миксоматоза и многоядерные клетки, подобные клеткам злокачественной гистиоцитомы.
Десмопластическая меланома обладает выраженным инфильтрирующим ростом с характерным нейротропизмом, но ее все-таки следует отличать от нейротропной меланомы.
Иммуногистохимически клетки десмопластической меланомы дают положительную реакцию на белок S-100 и отрицательную на НМВ-45.
Дифференциальный диагноз беспигментных вариантов десмопластической меланомы проводят со злокачественной эпителиоидной шванномой, а при наличии пигмента — со злокачественной меланоцитарной шванномой. Если опухоль связана с эпидермисом и распространяется на сосочковый слой дермы, то скорее всего это десмопластическая меланома или нейротропная десмопластическая меланома. Если же опухоль расположена глубоко в дерме или в мягких тканях, то более вероятно, что она шванновского происхождения. Если в опухоли отсутствуют митозы и нет ядерной атипии. то это десмопластический доброкачественный Spitz невус.
В некоторых десмопластических меланомах можно встретить один или два митоза в нескольких срезах, такие низкозлокачественные опухоли могут быть расценены как один из вариантов минимально отклоненной меланомы.
В Гистологической классификации опухолей кожи (ВОЗ, 1996г.) нейротропная меланома и минимально отклоненная меланома выделены как самостоятельные формы.
Десмопластическая реакция что это
ДЛЯ ТОГО ЧТОБЫ СКАЧАТЬ СТАТЬЮ В ФОРМАТЕ PDF ВАМ НЕОБХОДИМО АВТОРИЗОВАТЬСЯ, ЛИБО ЗАРЕГИСТРИРОВАТЬСЯ
Цель исследования – определить гистогенез анапластических участков опухоли и окружающей стромы при протоковом раке поджелудочной железы. Установлено, что эпителиально-стромальные взаимодействия при протоковом раке поджелудочной железы обуславливают его агрессивное биологическое поведение, резистентность к химиотерапевтическому лечению и различную выживаемость в зависимости от степени дифференцировки опухоли. Гетерогенность протокового рака проявляется в появлении анапластического (саркомоподобного) компонента, в котором прослеживается способность эпителиальных опухолевых клеток приобретать свойство мезенхимальных клеток, не требующих наличия стромы для своего развития и обладающих агрессивным злокачественным потенциалом, влияющим на выживаемость больных.
Цель исследования – определить гистогенез анапластических участков опухоли и окружающей стромы при протоковом раке поджелудочной железы.
Материал и методы
Выполнен анализ операционного материала от 118 больных протоковой аденокарциномой поджелудочной железы (ПАК ПЖ), находившихся на лечении в медицинских учреждениях г. Москвы в период с 2005 по 2013 гг. Среди больных ПАК ПЖ преобладали мужчины (1,3:1). Возраст больных колебался от 40 до 80 лет. Средний возраст мужчин – 61 год, средний возраст женщин – 52 года.
Материал фиксировали в 10% забуференном растворе формалина, затем заливали в парафин по обычной методике. Серийные парафиновые срезы толщиной 3 мкм депарафинировали по стандартной схеме, окрашивали гематоксилином и эозином. Иммуногистохимическое исследование проводили на серийных парафиновых срезах толщиной 2 мкм по стандартой методике с применением следующей панели поликлональных антител: р63, кальпонин, гладкомышечный актин (ГМА), общий цитокератин, цитокератин 7, виментин, Е-кадгерин (Dako, LabVisionFlex, Дания). Интенсивность пероксидазной метки оценивали полуколичественным методом с учетом интенсивности окрашивания и количества антиген-позитивных клеток. Иммуногистохимическая реакция оценивалась как негативная («−» – нет реакции), слабопозитивная («+» – 10% клеток средней интенсивности окраски) и выраженная («+++» – >50% клеток высокой интенсивности окраски). Для проведения ИГХ-реакции применялась техника tissuemicroarrays (TMA), сконструированная в формате multitumorarrays. Данная модель состояла из 24 образцов первичной опухоли от разных больных, при этом от одного больного использовались образцы с разной степенью дифференцировки опухолевых клеток. Таким образом, это позволило осуществить скрининг определенного молекулярного повреждения во всем разнообразии представленных опухолей с наименьшей затратой реактивов и времени. Для получения цветного изображения использовали сканер Miraxdesk (Zeiss, Германия).
Результаты
Протоковая аденокарцинома поджелудочной железы имеет вид узла неправильной формы без четких границ, размерами от 2 до 10 см, на разрезе матового белесовато-серого или беловатожелтого цвета, каменистой плотности. Нередко в центре опухоли можно обнаружить очаги распада с формированием полостей различной формы. В большинстве случаев 78,8% (93 из 118) опухоль представлена железистыми структурами неправильной формы, состоящими из опухолевых клеток с различным содержанием муцина, выраженной десмопластической реакцией стромы, как правило, занимающей большую долю опухолевой массы (от 50–80%).
Однако в 21,2% (25 из 118) случаев в классическом гистологическом варианте ПАК ПЖ в опухоли наряду с железистыми структурами обнаружен анапластический (саркомо-подобный) компонент, представленный крупными полиморфными или веретенообразными клетками с гиперхромными ядрами, иногда многоядерными, с минимальным стромальным компонентом (рис. 1). Объем анапластического компонента разнился и составил от 5 до 20% общей массы опухоли, но во всех случаях не являлся преобладающим.
При проведении ИГХ-реакции обнаружены различия в экспрессии маркеров в железистом и анапластическом компонентах ПАК ПЖ. Так, выраженная экспрессия гладкомышечного актина (+++) отмечена только в десмопластической строме, окружающей железистые структуры. В опухолях с анапластическим компонентом также отмечена выраженная положительная реакция с ГМА, выявленная как в гладкомышечных волокнах, так и в единичных крупных анапластических опухолевых клетках. Помимо этого, как в строме, так и в эпителиальном анапластическом компоненте отмечена выраженная диффузная реакция с виментином (+++) (рис. 2), отсутствующая в железистых структурах (рис. 3). Одновременно в отдельных анапластических клетках отмечалась потеря экспрессии общего цитокератина и цитокератина 7 при сохраненной экспрессии эпителиального-мембранного антигена. Также, в ядрах анапластических клеток отмечена положительная реакция с р63, который может рассматриваться как маркер базальных стволовых клеток (рис. 4).
В опухолях без анапластического компонента, доля окрашенных ядер с антителами к р63 была ниже и представлена единично окрашенными ядрами по периферии железистых структур. Также при раке поджелудочной железы происходила редукция экспрессии белка Е-кадгерина и изменение полярности его экспрессии, а именно исчезновение мембранного окрашивания и появление цитоплазматического с разной степенью интенсивности. В опухолевых клетках железистых структур ПАК в 66,7% (62 из 93 случаев) наблюдалась умеренно-выраженная (++) цитоплазматическая экспрессия данного белка; в 30,1% (28 из 93) – выраженная цитоплазматическая (+++). Мембранная реакция наблюдалась только в 3,2% (3 из 93) случаев. В анапластическом компоненте во всех случаях отмечена отрицательная как мембранная, так и цитоплазматическая экспрессия белка Е-кадгерина.
Заключение
Классический вариант протоковой аденокарциномы поджелудочной железы по своей гистологической структуре, как правило, неоднородная опухоль, которая представлена полями ткани различной дифференцировки от высокой до низкой, включая анапластический компонент. В исследуемой серии анапластический компонент присутствовал в 21,2% (25 из 118) случаев. По нашему убеждению, его необходимо выделять даже при минимальном его объеме от общей массы опухоли, поскольку опухоли с анапластическим компонентом имеют не только различия в гистологическом строении, но и в злокачественном потенциале, а также по экспрессии эпителиальных, миоэпителиальных и мезенхимальных иммуногистохимических маркеров. Гистологически десмоплазия стромы, которая характерна для протокового рака поджелудочной железы, полностью отсутствует в анапластических участках. Опухолевые клетки, плотно располагаясь друг к другу, как бы создают «стромальный каркас» из самих себя (рис. 5).
Таким образом, возрастающий интерес исследователей к эпителиально-стромальным взаимодействиям в протоковом раке поджелудочной железы обусловлен его агрессивным биологическим поведением, резистентностью к химиотерапевтическому лечению и различной выживаемостью в зависимости от дифференцировки опухоли. Гетерогенность протокового рака проявляется в появлении анапластического (саркомоподобного) компонента, в котором прослеживается способность эпителиальных опухолевых клеток приобретать свойство мезенхимальных клеток, не требующих стромы и обладающих агрессивным злокачественным потенциалом, влияющим на выживаемость больных.
Десмоидные фибромы
В зависимости от локализации выделяют:
Причины возникновения десмоидных фибром
Как правило, пациенты обращаются к врачу по поводу безболезненного опухолевого образования, болевые ощущения и другие симптомы обычно связаны с вовлечением в опухолевый процесс близлежащих структур. Большинство пациентов с десмоидными фибромами экстраабдоминальной локализации связывают появление опухоли с предшествующей травмой. Десмоидные фибромы абдоминальной локализации зачастую развиваются у женщин после беременности или кесарева сечения. Интраабдоминальные десмоидные фибромы чаще всего сочетаются с полипозом толстой кишки (синдрома Гарднера).
Десмоидные фибромы-диагностика
Десмоидная фиброма-лечение
Группа специалистов (хирурги, радиологи, онкологи, морфологи) задействованы в лечении опухоли. После постановки диагноза десмоидная фиброма вариант лечения подбирается индивидуально для каждого пациента. К числу доступных вариантов лечения пациентов относятся динамическое наблюдение, хирургическое лечение, лучевая терапия и системная терапия (гормональные препараты, химиотерапия).
В зависимости от локализации опухоли возможны различные варианты хирургического лечения. Для достижения лучших онкологических и косметических результатов применяются различные виды пластики послеоперационного дефекта после удаления опухли.
При абдоминальных десмоидных фибромах пластика производится композитной сеткой. При экстраабдоминальной локализации опухоли в качестве пластического компонента могут быть использованы местные ткани, перемещенные или пересажанные лоскуты, а также различные виды модульных эндопротезов в случае вовлечения кости в опухолевый процесс. Помимо хирургического лечения в нашем Институте изучены и внедрены в практику эффективные схемы системного лекарственного лечения, а также лучевая терапия. Все описанные выше методы лечения могут применятся как отдельно, так и в комбинации для достижения наилучшего результата.
Десмоидная фиброма-прогноз заболевания
Так как десмоидные фибромы не относятся к злокачественным опухолям, прогноз заболевания благоприятный. Проведение радикальной операции позволяет снизить риск рецидива.
Филиалы и отделения, где лечат десмоидные фибромы
МНИОИ им. П.А. Герцена – филиал ФГБУ «НМИЦ радиологии» Минздрава России.
Отделение хирургического лечения центральной нервной и костно-мышечной систем
Врач-онколог ЯДРИНА Анна Викторовна
Интерстициальная болезнь легких (часть 2)
Стенограмма выступления академика РАМН, профессора Ивашкина В.Т. на II Международном Интернет Конгрессе специалистов по внутренним болезням. Часть 2.
Академик Ивашкин В.Т.: – Давайте посмотрим, в чем особенность бронхиолоальвеолярноклеточной карциномы. Многоликость бронхиолоальвеолярноклеточной карциномы. Частота этой опухоли возросла с 5% до 24%, следовательно, это часто встречающаяся опухоль легких. Эта опухоль – это подтип аденокарциномы с внутриальвеолярным распространением и ростом вдоль интактного итерстиция, но с наличием отчетливой стромальной, сосудистой и плевральной инвазии. Сопоставьте то, что вы уже видели – это точно укладывается.
Подтипы бронхиолоальвеолярноклеточной карциномы: муцинозный, немуцинозный, смешанный. У нашей пациентки был участок муцинозной и немуцинозной злокачественной трансформации, следовательно, у нашей пациентки была смешанная морфологическая форма бронхиолоальвеолярноклеточной карциномы. Какие отличительные особенности? Периферическая локализация – то, что было у нашей пациентки; ассоциация с десмопластической реакцией – то же самое, реакция плевры; продукция муцина; высокая частота среди некурящих – наша пациентка не курила; более высокая частота среди женщин; и тенденция к мультифокальности – до 25%, в то время как у других не мелкоклеточных карцином легких лишь 5% такая мультифокальность. Три разных радиологических варианта бронхиолоальвеолярноклеточной карциномы встречают клиницисты. Это солитарный узел или инфильтрат варьирующей плотности, фокальная консолидация и мультифокальный или диффузный процесс. Наша пациентка, по всей вероятности, все-таки относится к форме фокальной консолидации. И контроль – у пациентки отмечался кашель, у пациентки была бронхорея и нарастающая одышка.
Теперь посмотрим солитарные узлы или инфильтраты. Наиболее общая особенность – это солитарный периферический, как показано на левой картинке, вы видите округлую тень, ближе к остальной плевре; это дольчатый или плохо отграниченный легочный узел, здесь хорошо видно справа; или инфильтрат солидной консистенции, как это видно в центре. Наиболее общими компьютерно-томографическими чертами являются псевдокавитация, гетерогенная аттенуация, нерегулярность краев с формированием звездчатости и плевральная реакция. Под псевдокавитацией понимается то, что на самом деле полость как таковая не формируется. Опухоль представляет собой реакцию, опухолевую реакцию вокруг остающегося островка легочной ткани, и этот остающийся островок легочной ткани создает вместе с муфтой опухолевого роста иллюзию каверны, полости, чего на самом деле нет. Здесь показана форма псевдокавитации, слева ближе к периферии видна псевдокавитирующая опухоль, и справа на снимке видна опухоль с разряженным центром, очень похожая на то, что мы видели у нашей пациентки.
Я возвращаюсь к нашей картинке. Посмотрите, я вам показал целую серию, и мы видим то, что у нашей пациентки и в декабре 2011 года, и в марте 2012 года, и мы видим то, что описано. То есть, в принципе клиницист, который бы искал, мог бы предположить, хотя это, конечно, непросто. При наличии уже доказанной интерстициальной болезни легких искать еще опухоль – намного легче предположить… Но все-таки, смотрите, фистончатость краев, реакция плевры, развитие разряженности, воздушная бронхограмма – все это характерные черты бронхиолоальвеолярноклеточной псевдоопухолевой формы, которую мы встретили у нашей больной. Что же должно заставить клинициста, рентгенолога заподозрить эту форму опухоли? Во-первых, нормальный сосудистый рисунок в узлах и зонах консолидации – ей не делали контрастное исследование. Далее, воздушная бронхограмма в узлах – то, что у нашей пациентки. Не разрешающиеся участки «лучистого матового стекла» с наличием или без признаков псевдокавитации. Не разрешающаяся консолидация и сочетание узлов и консолидации – то, что было у нашей пациентки. Следовательно, в принципе диагноз этот возможен, и это надо критично оценить.
Теперь острый респираторный дистресс-синдром с формированием гиалиновых и интраальвеолярных мембран. Каким образом, почему он развился? Вначале дадим определение. Еще в 1971 году Ashbaugh дал такое определение: в острый респираторный дистресс-синдром входит острая одышка, тахипноэ, входит цианоз, рефрактерный к оксигенотерапии, что было у нашей пациентки, диффузные альвеолярные инфильтраты. Мы, к сожалению, не видели последний этап болезни, но, по всей вероятности, судя по морфологической картине, у нашей пациентки были диффузные альвеолярные инфильтраты. Далее, ателектазы, застой в легочных сосудах, кровоизлияния, отек легких, гиалиновые мембраны – это все подтвердили морфологи. Еще одно определение, Американского респираторного общества, оно говорит о том, что в определение входит наличие двусторонних альвеолярных инфильтратов и, что важно, нет признаков левопредсердной гипертензии. И мы на электрокардиограмме показали, что не было признаков, а были признаки перегрузки правых отделов сердца, что как раз характерно для острого респираторного дистресс-синдрома. Острый респираторный дистресс-синдром может быть следствием или прямого повреждения легких, или непрямого. Наиболее частыми причинами прямого повреждения легких могут быть пневмония или аспирация желудочного сока, а непрямого повреждения – сепсис или тяжелая травма с шоком и множественными трансфузиями. Но у нашей пациентки не было ничего из этих наиболее часто встречающихся причин.
Что же могло вызвать у нее развитие острого респираторного дистресс-синдрома? Давайте посмотрим. Была проведена блестящая работа, Heptinne и соавторы, и она совершенно недавно опубликована в Critical Care Medicine. Это было исследование легочной патологии post mortem у лиц, умерших с клиникой острого респираторного дистресс-синдрома. Исследователи взяли 376 пациентов с острым респираторным дистресс-синдромом, которые поступили в клинику. 207 из них выжило, 169 умерло. Из 169 100 были похоронены без аутопсии, а у 69 была проведена аутопсия. У 5 не были получены полные данные, поэтому на исследование пошло 64 умерших. Это очень большая группа, мы консультировались с морфологами, они все подтверждают, что это очень серьезная работа. И вот что нашли эти замечательные морфологи. Во-первых, они изучали диффузные поражения альвеол, и оказалось, что двустороннее поражение наблюдалось у 50% исследованных и региональное у 31%, а у лиц с двусторонним поражением в стадии экссудации было 25% и в стадии организации 25%. То есть, речь шла или об альвеолите, или об альвеолите с формированием фиброза. Диффузное поражение альвеол могло наблюдаться, ассоциируясь с другими заболеваниями, это почти 20%. Во-первых, с пневмонией или бронхопневмонией – 4, легочный инвазивный аспергиллез – 4, Pneumocystis carinii пневмония – 1, инфаркт миокарда, застой в легких, лимфоангиолейомиоматоз с микротромбозами. У нашей пациентки ничего из этих заболеваний не было.
Идем дальше. Что же все-таки нашли наши патологи? Выявилось, что существуют другие заболевания, не ассоциированные с диффузным повреждением альвеол, которые могут вызвать острый респираторный дистресс-синдром. Я перечисляю, это пневмония и бронхопневмония, застой в легких, легочный инвазивный аспергиллез. Обратите внимание, три положения помечены Nota Bene: хронические неспецифические воспалительные изменения, обычная интерстициальная пневмония – та пневмония, которая была диагностирована у нашей пациентки, – и облитеррирующий бронхиолит с организующейся пневмонией. То есть, три формы интерстициальной болезни легких могут служить причиной развития острого респираторного дистресс-синдрома. У нашей пациентки обычная интерстициальная пневмония.
Участвовала ли в формировании острого респираторного дистресс-синдрома опухоль? Этот вопрос остается без ответа, поскольку в этом очень тщательно выполненном исследовании нет ни одного пациента с опухолью легкого, у которого бы развился острый респираторный дистресс-синдром. Отсюда мы – осторожно все-таки – делаем заключение, что причиной развития острого респираторного дистресс-синдрома у нашей пациентки послужила прогрессирующая интерстициальная болезнь легких, которая закончилась финально присоединением острого респираторного дистресс-синдрома. Давайте посмотрим дальше. Вот как выглядит острый респираторный дистресс-синдром. Здесь видно – это острый респираторный дистресс-синдром на фоне грам-отрицательного сепсиса, двусторонние диффузные тени, указывающие на отек легких.
Вот 60-летний пациент. Острый респираторный дистресс-синдром и механическая вентиляция легких в течение 7 дней, и ретикулярные тени, что указывает на развитие фиброзирующего альвеолита. Следовательно, это, как морфологи говорят, стадия формирования фиброза у пациента с острым респираторным дистресс-синдромом. Вот компьютерная томограмма, острая фаза острого респираторного дистресс-синдрома. Двусторонние альвеолярные тени в задних легочных зонах. Это компьютерная томография получена уже в фазу фиброзирования-альвеолита, то есть, и альвеолит, и фиброзирование. И большая булла в правом переднем поле легкого. Самое главное – морфологические изменения, они очень похожи на те изменения, которые обнаружили наши морфологи. Видите, на левой картинке видны гиалиновые мембраны, а на правой картинке голубые поля – выраженный фиброз. Следовательно, речь идет о параллельно идущих изменениях: о тяжелых внутриальвеолярных изменениях, которые по существу делают невозможной оксигенацию, потому что слущенный эпителий альвеол заменен гиалиновыми мембранами, и интерстициальные зоны все трансформируются в очаги фиброза.
Здесь на левом снимке это альвеола, вы видите, что альвеола практически потеряла значительную часть эндотелиальных клеток, и одновременно резко диффузно изменены эпителиациты альвеол. Справа видно восстановление альвеолярного покрытия альвеолоцитами, видимо, процесс восстановления. Заключительная картинка – это схема из The New England Journal of Medicine. В правом верхнем углу на этой картинке показана зона альвеолярной стенки, практически лишенная альвеолоцитов, и вместо альвеолоцитов здесь идет замещение гиалиновыми мембранами. И мы видим также и толщину стенки, конечно, она совершенно недоступна для газообмена. И мы видим в этом процессе участие большого количества цитокинов, лимфокинов и так далее. Следовательно, это сложный процесс. И заключая наш экскурс в это печальное, но в то же время чрезвычайно поучительное клиническое наблюдение, мы должны с вами помнить о том, что случаи такой комплексной легочной патологии, конечно, требуют отчетливой мобилизации знаний врача и привлечения всех возможных средств лечения.
Таким образом, эта пациентка, молодая пациентка, женщина с интерстициальной болезнью легких по несчастью попадает в разряд пациентов, у которых развивается бронхиолоальвеолярноклеточная карцинома в форме псевдокавитации и с множественными метастазами. И на фоне этой комбинации интерстициальной пневмонии и бронхиолоальвеолярноклеточной карциномы развивается острый, острейший респираторный дистресс-синдром, от которого наша пациентка погибает. Это наблюдение, на мой взгляд, должно нас о многом заставить задуматься.
Как в данном случае дифференцировать перегрузку правых отделов сердца и исключить проявление добавления мелкоочагового инфаркта задней стенки? Понимаете, надо учитывать совокупность данных, когда мы наблюдаем подобную картину. У нас на глазах развивается острая дыхательная недостаточность, у нас на глазах развивается диффузный цианоз. У нас на глазах меняется электрокардиографическая картина. У нас на глазах падает сатурация кислородом. И при этом наша пациентка не демонстрирует признаков левожелудочковой недостаточности. Поэтому оценка кардиограммы в подобных случаях требует совокупной оценки всей клинической картины. Поэтому изолированный анализ электрокардиограммы у таких пациенток будет носить схоластический характер. Поэтому я думаю, что здесь вполне достаточно оснований для того, чтобы заключить об острой перегрузке правых отделов сердца.
Как часто в вашей практике встречаются пациенты с интерстициальной болезнью легких? В моей конкретно практике, я должен сказать, что я в медицине уже больше 50 лет. На заре моей врачебной деятельности диагноз «идиопатический легочный фиброз» был большой редкостью и вызывал внимание всей клиники. Он вызывал внимание госпиталя, идиопатический легочный фиброз. Эти пациенты всегда попадали в фокус внимания – проводились клинические разборы и так далее. В настоящее время, скажем, в пульмонологическом отделении нашей клиники интерстициальное заболевание легких занимает какой процент?
При своевременной диагностике тактика ведения? Я думаю, что даже если бы мы до развития острого респираторного дистресс-синдрома поставили диагноз злокачественной опухоли, это не повлияло бы на исход. Но это – я все время подчеркиваю – это не оправдание. Повлияло – не повлияло, врач должен ставить диагноз до того, как пациент направляется на секцию. Сегодня это бы не повлияло, а завтра, через год, через три, в подобной же ситуации, если бы мы поставили диагноз до развития острого респираторного, это может уже влиять на исход заболевания. Ушакова Ирина спрашивает, без компьютерной томографии нельзя было бы так четко? Конечно, безусловно. Это тот случай, когда без имидж-диагностики – как Александр Григорьевич Чучалин любит говорить, имидж-диагностика – заподозрить подобную форму опухоли, конечно, невозможно. Спасибо за внимание.