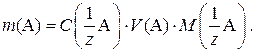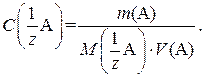Стандартизация решений в том, что состоит и решаемых упражнений
стандартизация решений это процесс, который позволяет точно определить концентрацию раствора. Вещества, используемые для этой цели, называются первичными стандартами..
Раствор стандартизируют, используя метод объемного титрования (титрование), либо классическими, либо инструментальными методами (потенциометрия, колориметрия и т. Д.)..
Для этого растворенные вещества заранее реагируют с тяжелым первичным стандартом. Поэтому использование объемных баллонов является обязательным условием для этих количественных анализов..
Например, карбонат натрия является основным стандартом, используемым при стандартизации кислот, включая соляную кислоту, которая становится титрантом, поскольку его можно использовать при титровании гидроксида натрия. Таким образом, основность выборки может быть определена.
Объемы титранта добавляются непрерывно, пока он не прореагирует с эквивалентной концентрацией аналита. Это указывает на то, что степень эквивалентности степени была достигнута; другими словами, титрант «нейтрализует» аналит полностью, превращая его в другой химический вид.
Известно, когда добавление титранта должно быть завершено с помощью индикаторов. Момент, в котором индикатор меняет цвет, называется конечной точкой титрования..
Что такое стандартизация?
Когда требуется большая точность в концентрации растворов, раствор для титрования стандартизируется так же, как и раствор, который она собирается назвать.
Реакции, в которых используется метод титрования, включают:
-Кислотно-основные реакции. Концентрация многих кислот и оснований может быть определена объемным методом.
-Реакции восстановления оксида. Химические реакции, включающие окисление, широко используются в объемном анализе; как например, йодометрические определения.
-Реакции осадков. Катион серебра осаждается вместе с анионом группы галогенов, таким как хлор, с получением хлорида серебра, AgCl.
-Реакции комплексообразования, например реакция серебра с цианид-ионом.
Характеристики первичных стандартов
Вещества, используемые в качестве основных стандартов, должны соответствовать ряду требований для выполнения их функции стандартизации:
-Имеют известный состав, так как в противном случае не будет точно известно, сколько следует взвесить из стандарта (не говоря уже о расчете его последующей концентрации).
-Быть стабильным при комнатной температуре и сопротивляться температурам, необходимым для сушки на плите, включая температуру, равную или превышающую температуру кипения воды.
-Имейте большую чистоту. В любом случае содержание примесей не должно превышать 0,01-0,02%. Кроме того, примеси могут быть определены качественно, что облегчит удаление возможных помех в анализах (например, ошибочные объемы используемого титранта).
-Быстро сохнет и не может быть настолько гигроскопичным, то есть удерживать воду во время сушки. И при этом они не должны терять вес при воздействии воздуха.
-Не поглощайте газы, которые могут вызвать помехи, а также вырождение рисунка
-Быстро и стехиометрически реагировать с реагентом-титрантом.
-Имеет высокий эквивалентный вес, который уменьшает ошибки, которые могут быть допущены при взвешивании вещества.
Стандартизация раствора титранта



Под стандартизацией раствора титранта имеют в виду установление его точной концентрации с относительной погрешностью, обычно не превышающей ± 0,1 %. Обязательным условием этой процедуры является высокая точность определения концентрации титранта.
приготовленные
установленныерастворы титрантов.
Приготовленныерастворы получают путем растворения точной навески тщательно очищенного исходного вещества в определенном объеме воды или другого растворителя (например, раствор NaCl, K2Cr2O7). Однако многие растворы таким путем приготовить нельзя, в том числе, NaOH, KMnO4. В таких случаях готовят раствор титранта приблизительной концентрации, а потом его стандартизуют, т. е. устанавливают концентрацию с необходимой точностью. Такие растворы называют установленными. Для стандартизации титрантов применяют специальные установочные вещества, так называемые первичные стандарты.
Первичные стандарты – вещества, имеющие состав, точно отвечающий химической формуле. Они должны удовлетворять следующим требованиям:
быть устойчивы на воздухе и иметь, по возможности, большую молярную массу эквивалента;
быть доступными, легко очищаться от примесей;
реакция вещества титранта с установочным веществом должна протекать быстро, количественно и стехиометрически.
Растворы NaOH и КОН часто стандартизуют по дифталату калия КНС8Н4О4 или дигидрату щавелевой кислоты Н2С2О4 · 2Н2О.
Растворы HCl и H2SO4 стандартизуют по карбонату натрия Na2СО3 или декагидрату тетрабората натрия Na2В4О7 ·10 Н2О.
Иногда для стандартизации используют вторичные стандарты. В качестве вторичных стандартов выступают титрованные растворы веществ, способных взаимодействовать с титрантом. Например, стандартизацию раствора HCl можно сделать по титрованному раствору NaOH.
Основное правило, которое необходимо помнить: стандартизация титранта и последующее выполнение анализа необходимо проводить в одних и тех же условиях, а для стандартизации использовать то же вещество, которое будет анализироваться в дальнейшем.
Стандартные растворы готовят в мерных колбах из фиксаналов, которые содержат точно фиксированное количество вещества, обычно 0,1 моль эквивалента.
При стандартизации растворов используют: 1) метод отдельных навесок; 2) метод пипетирования.
Метод отдельных навесок
Рассчитывают массу навески стандартного вещества при условии, что расход титранта на её титрование составляет не более 20 мл. На аналитических весах взвешивают в бюксах три навески, которые могут отличаться от рассчитанной на ± 10 %. Затем их переносят точно в конические колбы для титрования, добавляют индикатор и титруют. Рассчитывают молярную концентрацию титранта для каждой навески стандартного вещества и расхождение между наибольшим и наименьшим результатами. Если расхождение не превышает 0.2 – 0.3 %, то берут среднее значение из всех трех результатов. В случае большего расхождения взвешивают еще одну навеску стандартного вещества, титруют её, находят четвертый результат и снова проверяют сходимость значений молярной концентрации
Метод пипетирования
При стандартизации растворов этим методом рассчитывают навеску стандартного вещества, необходимую для приготовления заданного объема раствора первичного стандарта с концентрацией, как правило. близкой к молярной концентрации титранта. Взвешенную на аналитических весах навеску твердого вещества количественно переносят в мерную колбу, растворяют, тщательно перемешивая. Аликвоту полученного раствора отбирают пипеткой, предварительно промытой этим раствором, в коническую колбу для титрования и титруют стандартизуемым раствором. Аликвота – порция вещества, содержащаяся в растворе, отобранном с помощью пипетки.
При стандартизации раствора титрование проводят не менее трех раз. Если объемы, затраченные на титрование, совпадают между собой в пределах 0,2 – 0,3 %, то берут из них среднее значение и рассчитывают молярную концентрацию титранта. В случае большего расхождения проводят повторное титрование.
Для приготовления стандартных растворов используют также «фиксаналы» (стандарт-титры). Фиксанал представляет собой стеклянную или пластиковую ампулу, содержащую точную навеску стандартного твердого вещества (или определенный объем титрованного раствора), необходимую для приготовления 1 литра точно 0.1 N раствора.

Кривые титрования
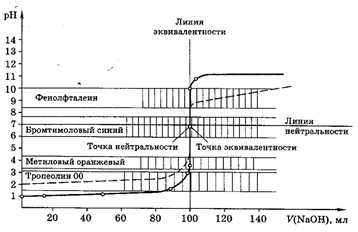
Кривые титрования являются важной характеристикой титриметрического метода. Они показывают графическую зависимость логарифма концентрации участника реакции, протекающей при титровании, или какого-то свойства раствора от объема добавленного титранта (или от степени оттитрованности). Например, для реакции кислотно-основного титрования: рН – V (объем титранта).
Кривая титрования служит для подбора индикатора, который позволит определить т.э. и т.к.т.
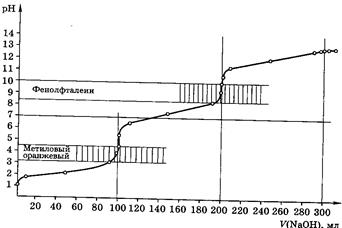
Рис 1. Кривая титрования 100,0 мл 0,1М НСl 0,1М раствором NaOH
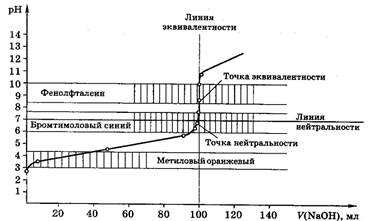
Рис 2. Кривая титрования 100,0 мл 0,1М СН3СООН 0,1М раствором NaOH
Рис 3. Кривая титрования смеси 0,1М НСl и 0,1М СН3СООН 0.1М раствором NaOH
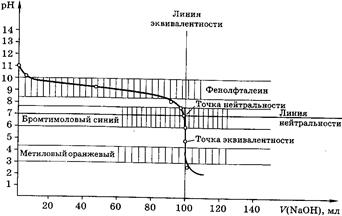
Рис 4. Кривая титрования 100,0 мл 0,1М NН3 0,1М раствором НСl
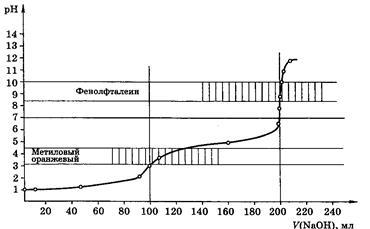
Рис 5. Кривая титрования 100,0мл 0,1М Н3РО4 0,1М раствором NaOH
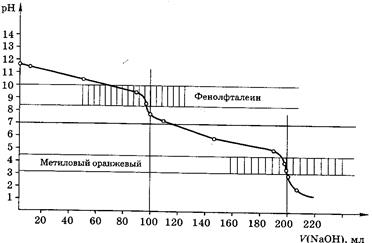
Рис 6. Кривая титрования 100,0мл 0,1М Na2СО3 0,1М раствором НСl
Стандартизация растворов титрантов


Стандартизация растворов титрантов
В таких случаях раствор для титрования готовят и стандартизируют, потому что его концентрация известна только приблизительно. Людмила Фирмаль
То есть концентрация установлена точно. Эти решения называются установленными. Для стандартизации решения используется специальный установочный материал — так называемый первичный стандарт. Эти вещества должны иметь состав, точно соответствующий химической формуле, быть стабильными на воздухе и, если возможно, соответствовать большой молярной массе.
Например, растворы iNaOH и KOH часто (KNS8N4O4) или дигидрат По раствору береновой кислоты НГСГО ^ НгО, HCI и H2SO4 fT ^ V — COOH Bifutaratu Na2CO3 борат или тетрагорат натрия декагидрат Na2B407 ‘• IOH2O, раствор перманганата калия — посредством. Часто для целей стандартизации используется вторичный стандарт, раствор для титрования вещества, которое может взаимодействовать с титром.
Оксалат натрия № 2 Cr04 и др. Людмила Фирмаль
Например, стандартизация раствора HCl может быть проведена с помощью титрованного раствора NaOH. Как правило, старайтесь стандартизировать титрант в тех же условиях, что и при проведении анализа, и, если возможно, использовать то же вещество, которое будет анализироваться в будущем.
Образовательный сайт для студентов и школьников
Копирование материалов сайта возможно только с указанием активной ссылки «www.lfirmal.com» в качестве источника.
© Фирмаль Людмила Анатольевна — официальный сайт преподавателя математического факультета Дальневосточного государственного физико-технического института
Стандартизация раствора титранта
Под стандартизацией раствора титранта имеют в виду установление его точной концентрации с относительной погрешностью, обычно не превышающей ± 0,1 %. Обязательным условием этой процедуры является высокая точность определения концентрации титранта.
· приготовленные
· установленные растворы титрантов.
Приготовленные растворы получают путем растворения точной навески тщательно очищенного исходного вещества в определенном объеме воды или другого растворителя (например, раствор NaCl, K2Cr2O7).
Однако многие растворы таким путем приготовить нельзя, в том числе, NaOH, KMnO4. В таких случаях готовят раствор титранта приблизительной концентрации, а потом его стандартизуют, т. е. устанавливают концентрацию с необходимой точностью. Такие растворы называют установленными.
Для стандартизации титрантов применяют специальные установочные вещества, так называемые первичные стандарты. Первичные стандарты – вещества, имеющие состав, точно отвечающий химической формуле. Они должны удовлетворять следующим требованиям:
· быть устойчивы на воздухе и иметь, по возможности, большую молярную массу эквивалента;
· должны быть негигроскопичны;
· быть доступными, иметь высокую чистоту (х.ч. или ч.д.а.), либо легко очищаться от примесей;
· реакция вещества титранта с установочным веществом должна протекать быстро, количественно и стехиометрически.
Растворы NaOH и КОН часто стандартизуют по дифталату калия КНС8Н4О4илидигидрату щавелевой кислоты Н2С2О4 · 2Н2О.
Растворы HCl и H2SO4 стандартизуют по карбонату натрия Na2СО3 или декагидратутетрабората натрия Na2В4О7 ·10 Н2О.
Иногда для стандартизации используют вторичные стандарты. В качестве вторичных стандартов выступают титрованные растворы веществ, способных взаимодействовать с титрантом. Например, стандартизацию раствора HCl можно сделать по титрованному раствору NaOH.
Основное правило, которое необходимо помнить: стандартизация титранта и последующее выполнение анализа необходимо проводить в одних и тех же условиях, а для стандартизации использовать то же вещество, которое будет анализироваться в дальнейшем.
Стандартные растворы готовят в мерных колбах из фиксаналов, которые содержат точно фиксированное количество вещества, обычно 0,1 моль эквивалента.
При стандартизации растворов используют: 1) метод отдельных навесок; 2) метод пипетирования.
1. Метод отдельных навесок.
Рассчитывают массу навески стандартного вещества при условии, что расход титранта на её титрование составляет не более 20 мл. На аналитических весах взвешивают в бюксах три навески, которые могут отличаться от рассчитанной на ± 10 %. Затем их переносят точно в конические колбы для титрования, добавляют индикатор и титруют. Рассчитывают молярную концентрацию титранта для каждой навески стандартного вещества и расхождение между наибольшим и наименьшим результатами. Если расхождение не превышает 0,2 – 0,3 %, то берут среднее значение из всех трех результатов. В случае большего расхождения взвешивают еще одну навеску стандартного вещества, титруют её, находят четвертый результат и снова проверяют сходимость значений молярной концентрации.
2. Метод пипетирования.
При стандартизации растворов этим методом рассчитывают навеску стандартного вещества, необходимую для приготовления заданного объема раствора первичного стандарта с концентрацией, близкой к молярной концентрации титранта. Взвешенную на аналитических весах навеску твердого вещества количественно переносят в мерную колбу, растворяют, тщательно перемешивая. Аликвоту полученного раствора отбирают пипеткой, предварительно промытой этим раствором, в коническую колбу для титрования и титруют стандартизуемым раствором. Аликвота – порция вещества, содержащаяся в растворе, отобранном с помощью пипетки.
При стандартизации раствора титрование проводят не менее трех раз. Если объемы, затраченные на титрование, совпадают между собой в пределах 0,2 – 0,3 %, то берут из них среднее значение и рассчитывают молярную концентрацию титранта. В случае большего расхождения проводят повторное титрование.
Для приготовления стандартных растворов используют также «фиксаналы» (стандарт-титры). Фиксанал представляет собой стеклянную или пластиковую ампулу, содержащую точную навеску стандартного твердого вещества (или определенный объем титрованного раствора), необходимую для приготовления 1 литра точно 0,1 моль/л раствора.
Приготовление и стандартизация рабочих растворов метода кислотно-основного титрования
Цель работы: приготовить и стандартизировать рабочие растворы метода кислотно-основного титрования – HCl и NaOH (или KOH).
Сущность работы. Для проведения титриметрического определения необходимо прежде всего приготовить стандартный (рабочий) раствор титранта.
Стандартные растворы готовят с использованием аналитических весов и точной мерной посуды (бюретки, пипетки, мерные колбы). Концентрацию их записывают с точностью до четвертой значащей цифры.
Классификация стандартных растворов и все возможные способы их приготовления представлены на схеме.
| Стандартные растворы | |||
| ¯ | ¯ | ||
| Первичные (приготовленные) | Вторичные (установленные) | ||
| ¯ | ¯ | ¯ | ¯ |
| Из стандартного исходного вещества | Из фиксанала | Из кристаллического вещества | Из более концентрированного раствора |
Первичный стандартный раствор можно приготовить сразу с точно известной концентрацией и не стандартизировать.
Способы приготовления первичных стандартных растворов:
Рис. 20. Приготовление первичного стандартного раствора
из кристаллического стандартного вещества
Ориентировочную массу навески вещества для приготовления раствора рассчитывают по формуле
После взятия навески и ее растворения в мерной колбе рассчитывают точную концентрацию приготовленного раствора по формуле
Кристаллическое вещество для приготовления первичного стандартного раствора должно соответствовать ряду требований:
– состав вещества должен строго соответствовать его формуле;
– вещество должно быть устойчиво на воздухе (не должно окисляться, поглощать СО2, Н2О) при хранении в твердом состоянии и в растворе;
– вещество должно быть хорошо растворимым, нелетучим, желательно безводным;
– вещество должно быть чистым (квалификации не ниже «х. ч.» или «ч. д. а», см. &);
– вещество должно легко очищаться от примесей перекристаллизацией;
– вещество должно иметь большую молярную массу эквивалента (тогда ошибка при взятии навески будет меньше);
– вещество должно быть доступным и недорогим.
Если взять такое вещество, взвесить его на аналитических весах и растворить в мерной колбе, то получится первичный стандартный раствор.

Поскольку чаще всего в ампуле содержится 0,1 моль-экв вещества, то концентрацию стандартного раствора, приготовленного из фиксанала в мерной колбе вместимостью V, находят по формуле
Вторичный стандартный растворготовят в два этапа.
1. Готовят раствор с примерно известной концентрацией из кристаллического вещества или из более концентрированного раствора, используя технические весы и мерную посуду с ориентировочными делениями (мерные цилиндры, стаканы с делениями).
2. Определяют его точную концентрацию (стандартизируют) путем титрования первичного стандартного раствора.
В лабораторной работе рабочие растворы HCl и NaOH готовят как вторичные стандарты путем разбавления более концентрированных растворов с последующей стандартизацией по первичным стандартным растворам тетрабората натрия Na2B4O7 ∙ 10H2O и щавелевой кислоты Н2С2O4 ×2H2O. При титровании протекают следующие реакции:
(fэкв(Na2B4O7) = 
(fэкв(Н2С2O4) = 
Концентрацию растворов установочных веществ задают близкой к концентрации рабочих растворов.
Оборудование и реактивы: технические и аналитические весы, электрическая плитка, мерные цилиндры (10–25 мл, 250 мл), стаканы с делениями (500 мл), денсиметр (ареометр), склянки с этикетками для хранения рабочих растворов, мерная колба, пипетка, бюретка, колбы для титрования, тигель, Na2B4O7 ×10H2O (х. ч.), Н2С2O4 ×2H2O (х. ч.), концентрированные растворы HCl и NaOH (или KOH), индикаторы метиловый оранжевый и фенолфталеин.
Выполнение работы
1. Приготовление разбавленных растворов HCl и NaOH:
– с помощью денсиметров измеряют плотности концентрированных растворов HCl и NaOH;
– по справочнику находят их молярные концентрации (моль/л);
– рассчитывают объемы концентрированных растворов HCl и NaOH, необходимые для приготовления 500 мл (или 300 мл по указанию преподавателя) 0,1 н. растворов;
– цилиндрами отмеряют рассчитанные объемы HCl и NaOH, переносят их в стаканы вместимостью 500 мл и разбавляют дистиллированной водой до нужного объема;
– приготовленные растворы HCl и NaOH переливают в подписанные склянки для хранения, закрывают пробками и тщательно перемешивают.
Приготовленные растворы HCl и NaOH имеет приблизительно известную концентрацию, поэтому их необходимо стандартизировать.
2. Приготовление первичного стандартного раствора Na2B4O7:
– рассчитывают ориентировочную массу установочного вещества Na2B4O7 ×10H2O, необходимую для приготовления 100 мл 0,1 н. раствора;
– установочное вещество взвешивают в тигле на технических, а затем на аналитических весах;
– навеску аккуратно пересыпают через воронку в мерную колбу, тигель с оставшимися на стенках частицами Na2B4O7 ×10H2O снова взвешивают на аналитических весах;
– по разности двух взвешиваний на аналитических весах находят массу Na2B4O7 ×10H2O, перенесенного в колбу;
– смывают навеску в колбу струей горячей дистиллированной воды, заполняют колбу на 2/3 объема водой. Снимают с колбы воронку и, перемешивая содержимое колбы круговыми движениями, добиваются полного растворения Na2B4O7 ×10H2O. Затем доводят содержимое колбы до метки дистиллированной водой и тщательно перемешивают раствор, многократно переворачивая колбу;
– вычисляют молярную концентрацию эквивалента Na2B4O7 с точностью до четвертой значащей цифры и приступают к титрованию.
3. Установление точной концентрации приготовленного раствора HCl (стандартизация):
– вымытую бюретку ополаскивают небольшим количеством приготовленного рабочего раствора HCl и заполняют ее этим раствором;
– в чистую коническую колбу переносят пипеткой определенный объем (аликвоту) приготовленного раствора установочного вещества Na2B4O7, прибавляют 1–2 капли индикатора метилового оранжевого и начинают титровать, перемешивая жидкость круговым движением колбы. Титрование прекращают, как только произойдет резкое изменение окраски раствора;
– титрование повторяют несколько раз, пока не будет получено не менее трех значений объема титранта, различающихся между собой не более чем на 0,1 мл. Все полученные результаты должны обязательно заноситься в лабораторный журнал, даже если они и одинаковые.
– рассчитывают средний объем титранта, учитывая только те значения, которые различаются не более чем на 0,1 мл;
– по результатам титрования находят точную молярную концентрацию эквивалента приготовленного рабочего раствора HCl.
В некоторых случаях по указанию преподавателя рабочий раствор HCl может быть приготовлен из фиксанала или установление концентрации его может быть проведено по стандартному раствору щелочи, Na2CO3 или NaHCO3.
4. Приготовление первичного стандартного раствора Н2С2O4:
– рассчитывают ориентировочную массу установочного вещества Н2С2O4×2H2O, необходимую для приготовления 100 мл 0,1 н. раствора;
– установочное вещество взвешивают в тигле на технических, а затем на аналитических весах;
– навеску аккуратно пересыпают через воронку в мерную колбу, тигель с оставшимися на стенках частицами Н2С2O4×2H2O снова взвешивают на аналитических весах;
– по разности двух взвешиваний на аналитических весах находят массу Н2С2O4×2H2O, перенесенной в колбу;
– смывают навеску в колбу струей дистиллированной воды, заполняют колбу на 2/3 объема водой. Снимают с колбы воронку и, перемешивая содержимое колбы круговыми движениями, добиваются полного растворения Н2С2O4×2H2O. Затем доводят содержимое колбы до метки дистиллированной водой и тщательно перемешивают раствор, многократно переворачивая колбу;
– вычисляют молярную концентрацию эквивалента Н2С2O4 с точностью до четвертой значащей цифры и приступают к титрованию.
5. Установление точной концентрации приготовленного раствора NaOH (стандартизация):
– вымытую бюретку ополаскивают небольшим количеством приготовленного рабочего раствора NaOH и заполняют ее этим раствором;
– в чистую коническую колбу переносят пипеткой определенный объем (аликвоту) приготовленного раствора установочного вещества Н2С2O4, прибавляют 1–2 капли индикатора фенолфталеина и начинают титровать, перемешивая жидкость круговым движением колбы. Титрование прекращают, как только появится неисчезающая розовая окраска раствора;
– титрование повторяют несколько раз, пока не будет получено не менее трех значений объема титранта, различающихся между собой не более чем на 0,1 мл. Все полученные результаты должны обязательно заноситься в лабораторный журнал, даже если они и одинаковые;
– рассчитывают средний объем титранта, учитывая только те значения, которые различаются не более чем на 0,1 мл;
– по результатам титрования находят точную молярную концентрацию эквивалента приготовленного рабочего раствора NaOH.
В некоторых случаях по указанию преподавателя рабочий раствор NaOH может быть приготовлен из фиксанала или установление концентрации его может быть проведено по стандартному раствору HCl.